賽默飛戰略合作伙伴 諾禾致源多基因檢測試劑盒獲批成功
發布時間:2018-08-19作者:賽默飛世爾科技(中國)有限公司
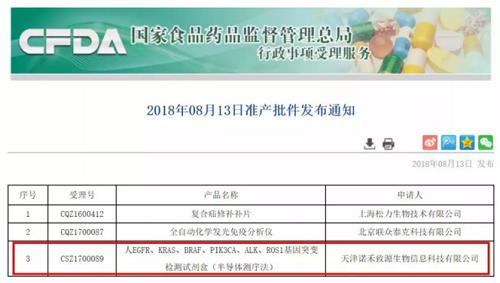
近日,國家藥品監督管理局通過創新醫療器械特別審批通道,批準天津諾禾致源生物信息科技有限公司“人EGFR、KRAS、BRAF、PIK3CA、ALK、ROS1基因突變檢測試劑盒(半導體測序法)”的三類醫療器械產品上市。
用于檢測非小細胞肺癌(NSCLC)患者腫瘤組織中與靶向治療密切相關的六個基因的突變狀態,篩選適合接受靶向藥物治療的患者。據悉,該試劑盒基于DA8600二代測序平臺,是目前國內唯一儀器和試劑均獲批的NGS腫瘤檢測系統。也是目前已獲批產品中基因數目最多、位點最多、報告周期最短的試劑盒。
中國臨床腫瘤學會《原發性肺癌診療指南》指出:
“ KRAS、PIK3CA突變與EGFR-TKI耐藥有關,可通過NGS技術進行檢測。諾禾致源的多基因檢測試劑盒覆蓋與NSCLC靶向治療用藥相關的六個基因,是目前CNDA批準的最多基因的腫瘤分子檢測試劑盒,全面提示患者治療相關的敏感、潛在耐藥及基因共突變信息,能夠準確提示基因豐度。”
與傳統基因檢測手段相比,基于NGS技術的多基因檢測試劑盒,只需一份組織樣本、一次檢測即可覆蓋多個腫瘤治療相關基因,實現點突變、插入缺失、重排(融合)等多種變異形式的檢測,為醫生和患者提供更全面的靶向治療的解決方案。
該多基因檢測試劑盒經過北京腫瘤醫院、北京胸科醫院、華西醫院、中國人民解放軍總醫院和河南省腫瘤醫院共5個中心2789例樣本的臨床試驗驗證。該檢測試劑盒與傳統金標準檢測方法的比較研究結果顯示,總符合率均在99%以上。
與吉非替尼、奧西替尼、克唑替尼伴隨診斷試劑的比較研究結果顯示,該多基因檢測試劑盒與原有伴隨診斷試劑具有良好的檢測一致性。與吉非替尼、奧西替尼、克唑替尼藥物療效相關的回顧性臨床研究結果顯示,根據該試劑盒檢測結果用藥的NSCLC患者,客觀緩解率(ORR)與既往藥物臨床試驗ORR相符。通過以上臨床性能的全面研究,充分證明了該多基因檢測試劑盒在NSCLC患者靶向治療用藥指導中的重要價值。
本次獲批上市的多基因檢測試劑盒基于擴增子建庫與半導體測序的技術體系開發,該技術體系已獲得國際認可。
基于該技術的儀器也就是DA8600高通量基因測序儀是由達安基因股份有限公司引進賽默飛的技術,在國內研發、生產、面向臨床應用的新一代高通量測序儀,已于2017年1月獲得國家食品藥品監督管理總局的注冊批準(國械注準20143401961),可以用于腫瘤和遺傳疾病等人體基因位點的檢測。
這是目前中國首臺由CFDA批準的可用于腫瘤和遺傳疾病臨床檢測的高通量測序儀,可廣泛應用于各醫療機構臨床檢測中心。
該儀器可實現從樣本提取到上機測序在一天內完成;
配合DA Chef系統,可實現全自動化模板制備和芯片上樣工作流程。
該儀器對環境要求相對較低、通量適中、檢測周期較短的優勢,特別適合在醫院內開展腫瘤檢測。2017年6月,基于該技術體系的OncomineDx Target Text試劑盒獲FDA批準上市,全球最大規模的臨床試驗NCI-MATCH也采用了該技術體系。

DA8600高通量基因測序儀
此次基于DA8600開發的多基因檢測試劑盒的獲批,是諾禾致源布局腫瘤NGS分子診斷領域的重要起點。此前,諾禾致源圍繞該檢測試劑盒進行了一系列的DNA提取備案,“癌癥基因數據處理軟件”III類醫療器械的申報等,結合此次多基因檢測試劑盒的獲批,力圖為醫院提供一站式腫瘤NGS分子病理診斷整體解決方案。
賽默飛作為諾禾致源的重要戰略合作伙伴,受邀出席了其上市發布會,祝賀諾禾致源實現此歷史性突破,未來賽默飛亦將全方位繼續支持諾禾致源在該領域的發展,持續提供穩定可靠的產品和服務,與諾禾致源一起致力于服務中國腫瘤患者人群,進而助力改善人類生活。
Copyright ? 2015 ilinki.net Inc. All rights reserved. 智匯工業版權所有
電話:010-62314658 郵箱:service@ilinki.net
 主辦單位:智匯萬聯(北京)信息技術有限公司
主辦單位:智匯萬聯(北京)信息技術有限公司

